MENU
La Alcalinidad en la Operación de sistemas de Tratamiento de Aguas Residuales
February 12, 2024

¿Sabe su operador que es la alcalinidad?
¿Sabe por qué?, cómo? y dónde medirla?,
¿Qué tan frecuentemente debe medirla
¿Qué sustancias utiliza el operador para añadir alcalinidad?
¿Sabe en qué dosis suminístrala?
–
LA ALCALINIDAD Y EL PH NO SON LA MISMA COSA…
La alcalinidad del agua es su capacidad para neutralizar ácidos. Es decir, ¿Cuánto ácido puede el agua absorber antes que se produzca un cambio importante en el pH?
La alcalinidad y el pH están relacionados, pero no miden la misma cosa. Alcalinidad es capacidad de amortiguación, el pH es concentración de iones de hidrogeno.
La alcalinidad está compuesta principalmente por los iones carbonato (CO3–), bicarbonato (HCO3–), hidróxidos (OH–).
Actualmente hay kits muy prácticos para medir la alcalinidad.
La siguiente gráfica nos muestra la cantidad y tipo de alcalinidad presente dependiendo del pH
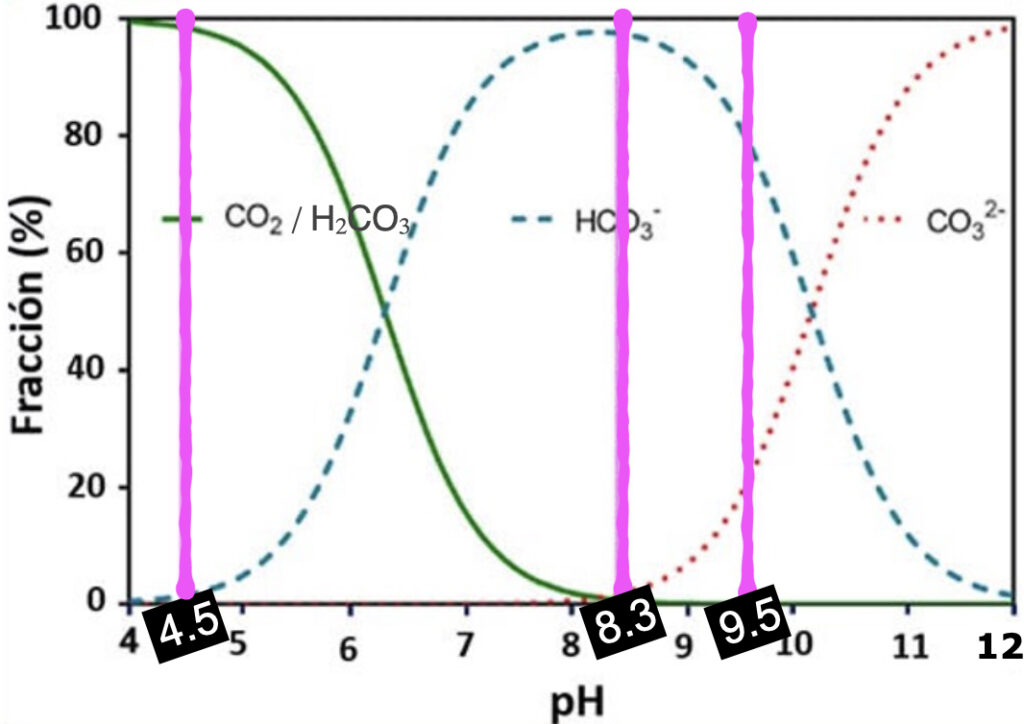
De la gráfica podemos obtener que:
- Debajo de un pH = 4.5, no hay alcalinidad presente ⛔️ 💀
- Entre un rango de pH [4.5 – 8.3] toda la alcalinidad presente es en forma de bicarbonato (HCO3–).
- Entre un rango de pH [8.3 – 9.5] toda la alcalinidad presente es en forma de bicarbonatos (HCO3–) y carbonatos (CO3–).
- A partir de un pH = 9.5 aparecen los hidróxidos (OH–).
–
¿DONDE EN UN SISTEMA DE TRATAMIENTO SE CONSUME ALCALINIDAD?
La alcalinidad es consumida durante los siguientes procesos en el tratamiento de aguas residuales:
- NITRIFICACIÓN: es el proceso de conversión de amoníaco a nitratos que se dan en los procesos aeróbicos con edad de lodos suficientemente larga.
- PRECIPITACIÓN de FÓSFORO: El aluminio y el hierro son comúnmente utilizados para la reducción del fósforo, reaccionando con los bicarbonatos en el agua residual formando hidróxidos de aluminio y de hierro.
- PREVENCIÓN de CAMBIOS en el pH: Procesos como la coagulación necesitan rangos estrechos y específicos de pH, por lo que se vuelve necesario la adición de químicos que añadan alcalinidad.
- CONDICIONES ANAEROBIAS: Los digestores y reactores anaeróbicos tienden a deprimir el pH por lo que mantener cierta cantidad mínima de alcalinidad es crítico para su buen desempeño. Adicionalmente condiciones anaerobias en el alcantarillado y sedimentadores primarios también pueden deprimir el pH.
–
¿QUE SUSTANCIAS PUEDE UTILIZAR EL OPERADOR PARA AÑADIR ALCALINIDAD?
Algunos de los químicos más utilizados por los operadores para añadir alcalinidad son:
Bicarbonato de sodio – NaHCO3.
Carbonato de sodio – Na2CO3.
Bicarbonato de calcio y magnesio – CaMg(CO3)2
Hidróxido de sodio (soda caustica) – Na(OH)
Hidróxido de calcio – Ca(OH)2
Hidróxido de magnesio (leche de magnesio) – Mg(OH)2
Óxido de calcio – CaO
El químico a utilizar dependerá de su:
Disponibilidad, costo, requerimientos de almacenaje y alimentación, seguridad, y la preferencia del operador. Adicionalmente si hay objetivos que pretende el operador además de aumentar la alcalinidad.
–
¿CON CUANTA ALCALINIDAD DEBERÍA OPERAR EL SISTEMA DE TRATAMIENTO?
La estabilidad de muchos procesos biológicos y químicos en el tratamiento de aguas residuales se dan en un rango estrecho de pH, y en vista que el pH está en una escala logarítmica, este puede cambiar rápidamente, degradando sustancialmente los procesos y haciendo difícil recuperar las condiciones normales, por lo que el monitoreo del pH debe de ser acompañado del monitoreo en la alcalinidad, por lo que se recomienda
nunca operar por debajo de una alcalinidad de 50 mg/l de CaCO3 y preferiblemente 100 mg/l de CaCO3.
–
ALGUNAS APLICACIONES
Se sabe que la aplicación de aluminio y de hierro consumen alcalinidad a una tasa de 0.5 mg/l y 0.56 mg/l por cada mg/l, respectivamente. Adicionalmente, el cloruro férrico es utilizado para el control de malos olores.
También se sabe que se consumen 7.14 mg/l de alcalinidad por cada 1 mg/l de amonio oxidado a nitratos en el tanque de aireación.
- En el proceso de nitrificación, ¿Cuánta alcalinidad será necesaria para convertir 20 mg/l de amoniaco (NH3) a Nitratos (NO3–)?
- 91 mg/l
- 243 mg/l
- 143 mg/l
- 192 mg/l
R/ Literal “c”. 7.14 mg/l (alcalinidad) x 20 mg/l NH3 = 142.8 ~ 143 mg/l de alcalinidad como Ca(CO3–) necesaria.
–
- Si toda la alcalinidad es consumida, ¿Cuál sería el pH?
- 1.2
- 4.5
- 7.0
- 8.3
R/ Literal “b”. Por definición, cuando el pH ha llegado a un valor de 4.55, toda la alcalinidad ha sido consumida.
–
- ¿Por qué razón el operador decidiría utilizar cloruro férrico en vez de sulfato de aluminio para precipitar el fosforo?
- Control de olores
- Control de filamentos
- Por precio
R/ Literal “a”. El aluminio y el hierro son comúnmente utilizados para la reducción del fósforo, con la característica que el cloruro férrico también se utiliza para controlar los malos olores.
–
- Por qué motivo algunas veces se añade cal al lodo luego de habérsele añadido cloruro férrico para su acondicionamiento.
- Para prevenir un descenso inaceptable en el pH
- Para reducir la producción de lodos
- Para activar completamente el cloruro férrico
R/ Literal “a”. En el pasado el cloruro férrico fue el acondicionador de lodos más popular pero dejo de serlo por incrementar el volumen de lodos. Sin embargo, se utilizaba posteriormente con la cal para prevenir un descenso inaceptable en el pH.
–
- Si el influente de una planta de tratamiento aeróbica tiene muy poca alcalinidad y esta debe reducir el amoniaco y también el fósforo ¿Cuál de los siguientes químicos sería la mejor opción?
- Cloruro férrico
- Sulfato ferroso
- Aluminato sódico
- Sulfato de aluminio
R/ Literal “c”. El aluminato sódico ya que este no consumiría alcalinidad la cual en este caso ya es baja.
–
- El añadir químicos para la precipitación del fósforo aguas abajo del sedimentador secundario, en una planta de tratamiento aeróbica, tendría la siguiente ventaja:
- Previene la conversión de hierro ferroso a hierro férrico
- Previene que la perdida de alcalinidad afecte al proceso de nitrificación.
- Incrementa las partículas finas en el efluente final.
R/ Literal “b”. Los químicos comúnmente utilizados para la precipitación del fosforo son el aluminio y el hierro, pero estos también consumen alcalinidad; por lo que al aplicarlos agua abajo del sedimentador secundario, aunque tiende a consumir alcalinidad, no afectaría el proceso de nitrificación que se da en el tanque de aireación.
–
FINALMENTE TOMAR EN CUENTA…
Las características del agua potable pueden influenciar la alcalinidad, la cual puede ser alta en áreas donde hay aguas duras (típicamente asociada al agua subterránea con altas cantidades disueltas de magnesio y calcio), y muy baja en áreas con agua suave.
Hay que recordar que la alcalinidad se mide en miligramos por litro de carbonato de calcio equivalente (mg/l CaCO3).